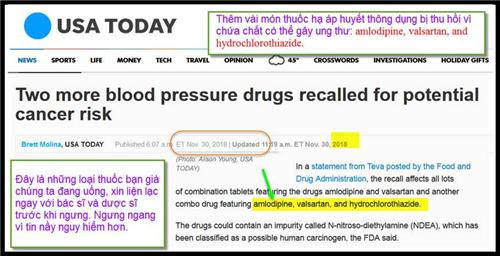
Teva Pharmaceuticals đã đưa ra thông báo thu hồi tự nguyện hai loại thuốc được sử dụng để điều trị bệnh cao huyết áp vì loại thuốc này đối mặt với mối lo ngại về nguy cơ ung thư có thể xảy ra. USA TODAY
Trong một tuyên bố từ Teva được đăng tải bởi Cục Quản lý Thực phẩm và Dược phẩm, việc thu hồi ảnh hưởng đến tất cả các viên thuốc kết hợp có chứa thuốc amlodipin và valsartan và một loại thuốc kết hợp khác có amlodipin, valsartan và hydrochlorothiazide.
Các loại thuốc có thể chứa một tạp chất được gọi là N-nitroso-diethylamine (NDEA), đã được phân loại như một chất có thể gây ung thư, FDA cho biết.
Bệnh nhân dùng thuốc nên liên hệ với bác sĩ hoặc dược sĩ của họ để được tư vấn hoặc điều trị thay thế. Ngừng thuốc ngay lập tức mà không có sự thay thế hoạc so sánh có thể gây ra nguy cơ lớn hơn đối với sức khỏe của bệnh nhân, Teva nói.
Khách hàng và bệnh nhân có thắc mắc có thể liên hệ với Teva qua điện thoại theo số 888-838-2872 hoặc gửi email tới druginfo@tevapharm.com.
Vào tháng Tám, FDA đã thông báo thu hồi valsartan vì các sản phẩm có thể chứa tạp chất. Tháng trước, có thêm hai vụ thu hồi đã được công bố: một cho thuốc irbesartan và thu hồi thứ hai cho thuốc viên losartan kali hydrochlorothiazide.
Trong một cuộc phỏng vấn vào tháng 11 với USA TODAY, ủy viên FDA Scott Gottlieb cho biết việc thu hồi thuốc huyết áp để tập trung vào chất lượng của thuốc để đảm bảo không có tạp chất.